В связи с углеводным обменом нужно заострить внимание читателей еще на двух вопросах, которые тесно связаны с таксономией. Прежде всего мы имеем в виду отношение Y. pestis к глицеролу. Как известно уже давно [Безсонова, 1928], по этому признаку различают две группы штаммов — глицериннегативные и глицеринпозитивные. В подавляющем большинстве случаев первые выделяются в тех очагах, где хранителями чумного микроба являются крысы («океанические» штаммы). Чаще всего оканические штаммы встречаются в очагах тропического пояса. Вторые же обычно выделяются от сусликов, сурков и песчанок. В связи с этим распространение глицеринпозитивных штаммов географически привязано к ареалам распространения указанных видов грызунов («континентальные» штаммы). По нашим данным [Домарадский И. В. и др., 1974], причина негативного отношения чумного микроба к глицерину может заключаться в утрате им только одного фермента — первого в цепи последующих, а именно глицеролдегидрогеназы. Однако чем объяснить подобную «диссоциацию» чумного микроба? особенностями обмена веществ его хозяев или какими-то другими факторами (абиотическими?), пока никто не знает.
Второй вопрос касается рамнозы. После того как А. А. Безсонова [1929] предложила среду с рамнозой для дифференциации Y. pestis от Y. pseudotuberculosis, отношение чумного микроба к этой пентозе стало предметом многочисленных исследований. При этом выяснилось, что неспособность ферментировать рамнозу является весьма постоянным признаком чумного микроба. Однако, как показала E. Englesberg [1957а], начиная с 6-го дня инкубации могут появляться рамнозопозитивные клоны, с частотой порядка 10–11, с чем и связана «поздняя» ферментация, которую подчас наблюдают в лабораториях. Продолжив изучение отношения к рамнозе, E. Englesberg [1957б] показала, что рамнозопозитивные мутанты чумного микроба окисляют эту пентозу только в том случае, если их предварительно выращивают в её присутствии. При выращивании же на среде с глюкозой окисление рамнозы начинается лишь после 50-минутного контакта с ней и максимальное потребление кислорода достигается к концу 2-го часа. Однако при этом рамноза окисляется неполностью, причём одним из продуктов распада является 2-оксипропионовый альдегид. У «адаптированных» рамнозопозитивных мутантов были обнаружены изомераза рамнозы, катализирующая её превращение в рамнулозу, и рамнулозокиназа.
Однако, помимо разложения рамнозы в поздние сроки, причина которого установлена E. Englesberg [1957а], встречаются случаи, когда оно регистрируется одновременно с ферментацией других углеводов; обычно с этим сталкиваются при работе со штаммами, выделенными в горных очагах. Чем объяснить эту особенность «горных» штаммов, сказать мы не можем.
Реакции переаминирования являются центральными реакциями в белковом обмене животных, растений и микроорганизмов. Поэтому неудивительно, что они выявлены и у чумного микроба [Оленичева Л. С., Атарова Г. Т., 1967]. Обращает на себя внимание то, что в отличие от Y. pseudotuberculosis, чумной микроб лишен γ-глутаматтрансферазы, (факт, представляющий интерес для их дифференциации [Bercovier H. et al., 1981]. Помимо трансаминаз, у Y. pestis обнаружены дезаминазы ряда аминокислот [Домарадский И. В., 1956] и декарбоксилаза аргинина. Наличие последней также важно для диагностики [Шиманюк Н. Я., 1972].
Показана способность чумного микроба превращать одни амнокислоты в другие, в частности орнитин в аргинин, аспартат в пролин, цистеин в метионин [Сучков Ю. Г. и др., 1971; Король В. В., 1973].
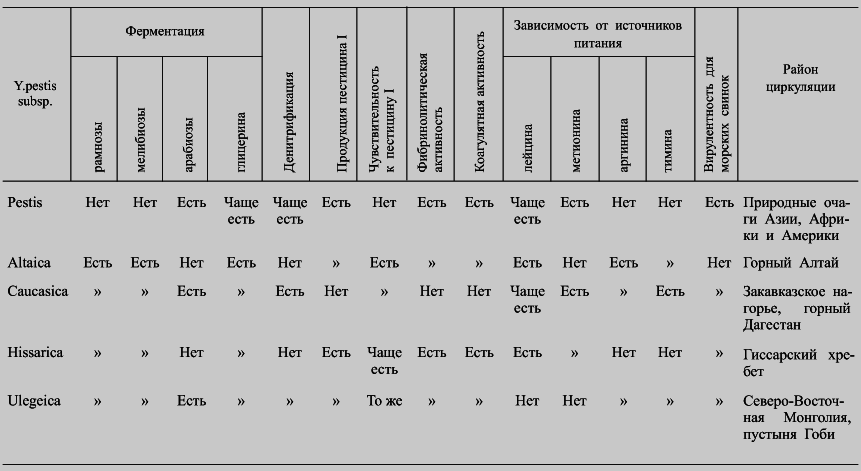
Все сказанное, вместе с независимостью от азотистых оснований и дополнительных факторов роста[9], объясняет относительную неприхотливость чумного микроба к питательным средам. Однако её степень во многом зависит от происхождения штаммов, что было подмечено нами [Домарадский И. В., 1956] и стало общепризнанным в результате работ И. Л. Мартиневского [1969]. В качестве примера связи потребности в аминокислотах с происхождением штаммов можно сослаться на данные, приведенные в табл. 13.
Из других азотистых соединений внимания заслуживает мочевина, отношение к которой давно уже помогает отличать чумной микроб от возбудителя псевдотуберкулеза. Правда, сомнения в надежности этого теста были посеяны Г. Н. Ленской [1944] и Е. Е. Пунским [1960], что было связано с несовершенством тогдашней методики определения уреазы, однако после специальных исследований нескольких сонен штаммов разного происхождения неспособность чумного микроба гидролизовать мочевину была признана непреложной истиной.
3.4. Вопросы таксономии
Как видно из приведенных выше фактов, по некоторым признакам одни штаммы чумного микроба отличаются от других, что с легкой руки R. Devignat [цит. по Pollitzer R., 1954] и В. М. Туманского [1958] послужило основанием для постулата о внутривидовой неоднородности чумного микроба. Исходя из этого постулата, одна за другой стали появляться схемы соответствующих классификаций, например Л. Н. Классовского и В. С. Петрова [1970], Л. А. Пейсахиса и В. М. Степанова, [1975], Л. А. Тимофеевой и А. И. Логачёва [1975], построенные в общем по одному принципу — на признании зависимости особенностей штаммов от видовой принадлежности носителя возбудителя чумы («зоологическая» классификация). Это привело к тому, что в 1985 г. на Всесоюзном совещании по таксономии чумного микроба была принята единая «систематическая схема подвидовых категорий для возбудителя чумы, о чём было сделано уведомление в Национальный центр по таксономии бактерий» [Наумов А. В., Самойлова Л. В., 1992]. «Универсальная» схема для определения подвидов чумного микроба, основанная на результатах определения коэффициентов подобия (S) между различными штаммами, отражена в табл. 13. Эта схема полнее, нежели другие, и удобнее для практики.
Наше отношение к подобным классификациям сформировалось более 25 лет назад и с тех пор не изменилось [Домарадский И. В., 1971]. Мы по-прежнему считаем, что известные теперь различия между штаммами не могут служить достаточно веским аргументом в пользу существования подвидов чумного микроба. Мы не понимаем, почему не признать наличие вариаций («биоваров» или «биотипов»), как это сделано, например, в случае Y. enterocolitica?
Следует также подчеркнуть, что все известные нам схемы внутривидовой классификации штаммов чумного микроба построены на результатах изучения штаммов из природных очагов СНГ и поэтому являются узкими, «национальными». К их составлению совершенно не привлекаются данные о штаммах из зарубежных природных очагов. Мы не исключаем, что, если следовать логике отечественных исследователей, то в таком случае число «подвидов» увеличилось бы в несколько раз!
И еще одно замечание. Делению на подвиды придают у нас такое большое значение, поскольку оно якобы позволяет внести больше ясности в проблему изучения природных очагов чумы и наметить «правильные пути «для их ликвидации [Туманский В. М., 1958]. Но ведь независимо от вида носителя и географической зоны выделения возбудителя чумы к ликвидации её очагов нужно стремиться всегда (мы имеем в виду не природный очаг, а очаг непосредствнного заражения людей). При этом важно не то, ферментирует ли микроб глицерин и восстанавливает нитраты, а в какой мере он способен вызывать чуму. Насколько нам известно, эпидемии чумы вызывали все (кроме полёвочьей?) «разновидности» чумного микроба, но отличия между ними определялись отнюдь не подобными признаками штаммов. Добавим, что в одних и тех же природных очагах могут циркулировать разные штаммы, а при пассажах через организм соответствующих видов грызунов одна «разновидность» может превращаться в другую.
Наконец, отметим, что многие систематики животных давно уже избегают пользоваться понятием «разновидность» [Ралль Ю. М., 1965; Завадский К. М., 1968]. Пора это сделать и микробиологам!
9
Зависимость от тиамина выявлена у штаммов горного происхождения [Наумов А. В., Самойлова Л. В., 1992].