Другие явления при чуме (исчезновение гликогена из печени, гипогликемия и повышение остаточного азота крови (также могут быть связаны с эндотоксином [Walker R. W., 1968; Walker R. W. et al., 1966]. Весьма вероятно, что эти изменения вызываются нарушениями функции почек и расстройством углеводного обмена, связанным с выбросом большого количества эпинефрина. При патологоанатомическом исследовании у животных наблюдаются поражения канальцев почек и жировая инфильтрация клеток печени. По данным M. S. Finegold [1968], в сосудах канальцев почек людей, погибших от чумы, часто видны тромбы и некрозы коркового вещества, напоминающие картину при общей реакции Шварцмана у кроликов.
Прямым доказательством участия эндотоксина в патогенезе чумы можно считать наличие его в крови больных в течение всего периода заболевания бубонной чумой, а у некоторых больных даже после клинического выздоровления [Butler T. et al., 1973]. Эндотоксин находили не только в крови, но и в цереброспинальной жидкости — при чумном менингите.
Этот вопрос уже служил предметом специального рассмотрения [Домарадский И. В., 1966]. Однако за истекшие с тех пор три десятилетия загадка осталась неразгаданной. Более того, никому так и не удалось воспроизвести данные авторов, упоминавшихся в начале главы. Поэтому одна из возможностей заключается в продолжении поиска ответ на вопрос с тех позиций, что» истинный» токсин образуется только in vivo и что он является весьма нестойким компонентом микробной клетки.
Многочисленные попытки найти связь между теми или иными свойствами бактерий и их вирулентностью чаще всего заканчиваются неудачей. Скорее всего, как мы неоднократно подчеркивали, это связано с тем, что свойства бактерий, о которых мы судим по результатам опытов in vitro, отличаются от свойств, приобретаемых бактериями in vivo [Домарадский И. В., 1996,1997][18]. Если это так, то факторы вирулентности столь же разнообразны, как и разнообразны видовые особенности микроорганизмов. К сожалению, это мнение разделяется далеко не всеми. Мы говорим «к сожалению», поскольку отрицание специфичности вирулентности, её видовой обусловленности, тормозит решение многих проблем инфекционной патологии. Исходя из этого вирулентность микроба следует рассматривать как функцию его способности адаптироваться к организму хозяина. В естественных условиях бактерии вынуждены перестраивать свой метаболизм таким образом, чтобы можно было противостоять защитным силам организма и чем сильнее выражена эта способность, тем больше вероятность развития инфекции. При этом бактерии приобретают, в частности, способность образовывать капсулу или токсин, которые не нужны им тогда, когда они попадают на искусственные питательные среды, изменять антигенность и даже прибегать к «антигенной» или «молекулярной» мимикрии. Однако чаще всего мы плохо представляем себе те изменения в метаболизме патогенных бактерий, которые помогают им выживать при смене среды обитания. И основной причиной этого являются методические трудности. Поэтому вполне вероятно, что «истинный» токсин, действующий на все виды лабораторных животных, чумной микроб образует только in vivo. Возможным подтверждением этого являются теперь забытые работы английских авторов, в частности, E. C. Cocking и соавт. (1960). Для выделения токсина они использовали клетки чумного микроба из перитонеальной и торокальной полостей 400 морских свинок, погибших от острой чумы и разрушали их ультразвуком. В итоге были получены препараты токсина, которые у морских свинок вызывали картину чумной интоксикации, часто наблюдаемой у людей. Еще одним доводом, свидетельствующим о том, что in vivo чумной микроб образует факторы патогенности (или вирулентности), не выявляемые у него in vitro, могут служить многочисленные данные о LCR-белках, кодируемых плазмидой pCad (cм. раздел 3.8.2). В данном случае особый интерес представляют результаты опытов G. Mazza и соавт. [1985]. Согласно этим результатам, в сыворотках крови иммунизированных животных (мышей, кроликов), как и у людей больных чумой, выявляются антитела по крайней мере к двум антигенам Y. pestis, которые in vitro у чумного микроба отсутствуют; Y. enterocolitica в отличие от чумного микроба синтезируют оба антигена во всех случаях.
Альтернативой сказанному, к чему мы все больше и больше подчас склоняемся, является предположение об отсутствие у чумного микроба мифического «истинного» токсина. В таком случае всю картину интоксикация при чуме можно объяснить потенцированием эффектов мышиного токсина и ЛПС при связывании их различными, но специфическими для каждого из них клетками-мишенями. Подтверждение этого усматривается в результатах недавних опытов В. Зюзина и соавт. [1997]. Ими было установлено, что дозы «мышиного» токсина и ЛПС, которые сами по себе не летальны для белых мышей и морских свинок, при совместном введении вызывают их гибель. Авторы этой работы делают вывод, что «мышиный» токсин и эндотоксин — единый «токсический комплекс», который в организме чувствительного к чуме хозяина» образуется de novo[19].
О большой способности чумного микроба распространяться в организме нетрудно судить хотя бы по данным Е. И. Коробковой [1956], согласно которым уже через 5-10 мин. после накожной или внутрикожной прививки даже вакцинного штамма EV чумной микроб обнаруживается в глубоких слоях кожи, подкожной клетчатке, регионарных лимфатических узлах, крови, легких, печени и селезенке (рис. 12). Естественно поэтому, давно уже возник вопрос о механизмах, обусловливающих такую способность.
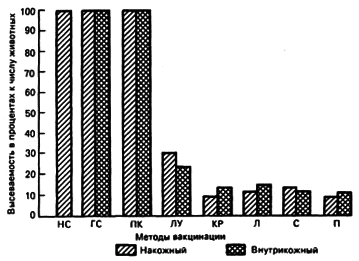
Рис. 12. Высеваемость вакцинного штамма ЕV из наружного (НС) и глубокого (ГС) слоев кожи, подкожной клетчатки (ПК), лимфатического узла (ЛУ), крови (КР), легких (Л), селезенки (С) и печени (П) после 5-минутного воздействия вакцины на скарифицированную кожу с последующим механическим удалением вакцины и иссечения депо вакцины через 5 мин после внутрикожной прививки [Коробкова Е.И., 1956].
E. Jawetz и K. Meyer [1944] показали, что в лизатах авирулентных и вирулентных штаммов чумного микроба содержится фактор, усиливающий проницаемость тканей и капилляров. У живых авирулентных штаммов этот фактор не обнаружен. По утверждению указанных авторов действие «фактора распространения» (ФР) в организме иммунных к чуме морских свинок выражено гораздо слабее, чем в организме неиммунных животных. Поскольку cпециально изучением ФР E. Jawetz и K. Meyer не занимались, каких-либо предположений о его природе они не высказали.
В отличие от американских авторов Е. И. Коробкова [1947] обнаружила ФР даже у цельных клеток чумного микроба, независимо от их вирулентности, хотя наибольшей активностью ФР обладали супернатанты агаровых культур. В то же время в опытах Е. И. Коробковой ФР выявлялся только при использовании неиммунных животных. В последующем Е. И. Коробкова [1950] пришла к выводу, что способность чумного микроба увеличивать площадь распространения красок в коже кроликов и морских свинок обусловлена наличием у него фермента, который она отождествила с гиалуронидазой, однако при тщательной проверке этого выявить гиалуронидазу у Y. pestis я и мои коллеги не смогли. Наши исследования проводились как в опытах in vitro, так и in vivo, с большим числом штаммов чумного микроба и параллельно с Staphylococcus aureus и Сlostridium perfringens, которые этим ферментом заведомо обладают. Скорее всего причина расхождений в результатах наших опытов и опытов Е. И. Коробковой заключались в том, что в её случае отсутствовали необходимые контроли [Домарадский И. В., 1966].
В чём же все-таки причина столь поразительной инвазивности чумного микроба? Весьма вероятно, что одна из причин кроется в наличии у чумного микроба нейраминидазы, обнаруженной Н. Я. Шиманюк и Б. Н. Мишанькиным [1982], которая при определенных условиях может восполнять отсутствие гиалуронидазы. Возможно также, что роль ФР у чумного микроба играют «фибринолизин» (активатор плазминогена, на что указывала еще Г. А. Яромюк[20], и пестицин 1, оказавшийся одной из гидролаз. Впрочем, при тех тяжёлых деструктивных изменениях в организме, в частности в крупных и мелких сосудах, что наблюдается при чуме всеми исследователями, путь для её возбудителя в лимфу и кровь всегда открыт.
18
Применительно к чумному микробу эту мысль впервые высказали Т. W. Burrows и G. A. Bacon [1956а, Ь].
19
Результаты опытов В. Зюзиной и соавт. (1997) очень напоминают результаты изучения действия поверхностно-активных веществ на токсичность чумного микроба [Pannell L., 1955; Goodner К. et al., 1955].
20
Об этом сообщали также R. Brubaker (1967), О. A. Sodeinde и соавт. (1992) и К. Kuusela (1996).