И вот у Рэмзэя мелькнула мысль: а что, если этот пузырек был вовсе не азот, а какой-то другой, не замеченный химиками газ, подмешанный к воздушному азоту? Верно, этот неизвестный газ – и есть та самая примесь, которая делает каждый литр воздушного азота на целых 6 миллиграммов тяжелее, чем литр азота из аммиака или селитры.
Но как узнать, верно это или нет? Как проверить эту догадку?
А вот как: если такой газ в самом деле существует, нужно во что бы то ни стало разлучить его с азотом.
Примесь найдена
Физик Рэлей и химик Рэмзэй заперлись в своих лабораториях и стали порознь решать задачу: как извлечь из воздушного азота спрятанную в нем примесь? Они условились не выходить из лабораторий до тех пор, пока неизвестная примесь не будет выделена. А для того, чтобы каждый знал, как идут дела у другого, они ежедневно обменивались через посыльного письмами и протоколами опытов.
Рэлей решил попросту повторить опыт Кэвендиша, но в гораздо больших размерах. Ему-то это было легко: ведь в его время физики располагали такими электрическими приборами, о которых Кэвендиш, за сто лет перед тем, не смел и мечтать. Если к азоту и в самом деле подмешан какой-то неизвестный газ, не соединяющийся с кислородом, то теперь возможно добыть не крошечный пузырек этого газа, как сделал Кэвендиш, а по крайней мере несколько кубических сантиметров. И тогда будет нетрудно изучить этот газ, узнать его химические свойства, взвесить его на точных весах.
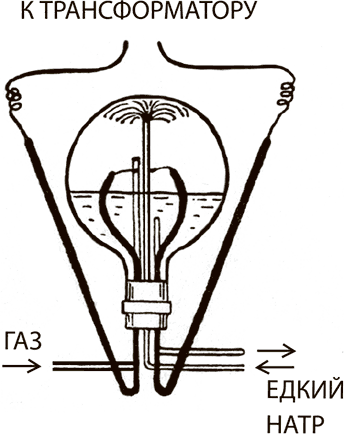
Рэлей взял стеклянный баллон и впаял в него две проволоки. Внутри баллона между концами проволок оставалось расстояние в несколько сантиметров. Наружные концы проволок торчали из баллона. Рэлей соединил их с высоковольтным трансформатором.
Когда будет включено электрическое напряжение, внутри баллона с кончика одной проволоки на кончик другой, через маленький промежуток в несколько сантиметров, поскачут электрические искры.
Рэлей накачал в баллон несколько литров азота и кислорода, а потом стал вгонять туда насосом раствор едкого натра. Едкий натр фонтаном врывался в баллон и вытекал из него по особой стеклянной трубочке.
В то же время Рэлей включил электрическое напряжение.
Посыпались искры, и под действием этих искр азот стал вступать в химическое соединение с кислородом. Рэлею только этого и надо было: он знал, что едва лишь азот соединится с кислородом, его можно будет выгнать из баллона с помощью едкого натра. Едкий натр – об этом писал и Кэвендиш – поглощает соединение азота с кислородом.
И в самом деле: через несколько часов весь азот, который был в баллоне, соединился с кислородом и ушел прочь из баллона вместе со струей едкого натра.
Азот ушел из баллона, но баллон не совсем опустел. На это указывал манометр – прибор, которым измеряют давление газа на стенки сосуда. Значит, в баллоне остался какой-то газ, – очевидно тот самый подмешанный к азоту газ, который так упорно искали Рэлей и Рэмзэй.
Этот газ не соединяется с кислородом, не растворяется в едком натре. Потому-то он и остался в баллоне.
Рэлей тщательно просушил и профильтровал новый газ, продувая его через фарфоровую трубку с горячими медными опилками. Горячие медные опилки очистили газ и от того ничтожного количества кислорода, которое все еще в нем оставалось.
Так Рэлей решил свою задачу – выделил неизвестный газ, подмешанный к азоту.
А как решил ту же задачу Рэмзэй?
Он поступил иначе. В его химической лаборатории не было высоковольтного трансформатора, какой был в лаборатории физика Рэлея. Но Рэмзэй был опытным химиком. Ему и без трансформатора удалось разлучить азот с неизвестным газом.
Он достал трубочку из тугоплавкого стекла, насыпал в нее кусочки магния и засунул ее в электрическую печку.
Когда печка нагрелась, кусочки магния раскалились докрасна.
Тогда Рэмзэй взял насос и стал гонять взад и вперед по этой трубочке азот, добытый из воздуха.
Раскаленный магний – это ловушка для азота: магний впитывает его в себя. Десять дней подряд гонял Рэмзэй по трубочке несколько литров азота. Наконец весь азот был поглощен раскаленным магнием.
Но в трубочке остался газ, который ни за что не соглашался соединиться с магнием.Рэлей и Рэмзэй шли разными путями, но пришли к одной и той же цели. Неизвестный газ был пойман, выделен, очищен и заперт в стеклянный баллон.
Ленивый газ
Оба ученых сейчас же принялись изучать новооткрытый газ. Наконец-то им удалось взвесить его на весах в чистом виде и узнать, правильна ли догадка Рэмзэя, что новый газ тяжелее, чем азот.
Да, тяжелее. Почти в полтора раза.
Так было объяснено расхождение в весе между «воздушным» и «аммиачным» азотом.
После этого Рэлей и Рэмзэй стали проделывать с новым газом всевозможные химические опыты. Они уже знали, что он не соединяется ни с кислородом, ни с магнием: ведь потому-то им и удалось извлечь его из азота.
Но с какими же веществами он соединяется?
Множество разных веществ испытали Рэлей и Рэмзэй. Они попробовали соединить новый газ с водородом, с хлором, с фтором, с металлами, с углем, с серой. Но всё было напрасно: газ упорно отказывался вступать в химическое соединение. Не помогло ни сильное нагревание, ни сжатие, ни электрические искры, ни прикосновение губчатой платины, – словом, ни один из многочисленных способов, которые применяют химики, чтобы заставлять вещества соединяться друг с другом.
В конце концов Рэлей и Рэмзэй вынуждены были прийти к заключению, что нет на свете такого вещества, с которым мог бы соединиться открытый ими газ.
Ученые еще никогда не встречали газа, обладающего таким странным свойством. Рэлей и Рэмзэй придумали для него название «аргон». По-гречески это значит «ленивый».
Победа точности
В августе 1894 года в старинном университетском городке Оксфорде состоялся съезд английских физиков, химиков, естествоиспытателей. На этом съезде Рэлей впервые рассказал о новом открытии. Его доклад вызвал удивление и недоверие. Еще бы! Каждый школьник знает, что воздух состоит из кислорода и азота. Так написано во всех учебниках. А Рэлей и Рэмзэй решаются утверждать, что в каждом литре воздуха, самого обыкновенного воздуха, того воздуха, которым мы дышим, есть еще девять кубических сантиметров нового, не замеченного химиками газа.
Девять кубических сантиметров на литр – это не так уже мало. «В каждом кубометре воздуха, – утверждал в своем докладе Рэлей, – содержится около пятнадцати граммов аргона. В зале, в котором заседает съезд, по этому расчету должно содержаться несколько пудов аргона».
С удивлением выслушали химики рассказ Рэлея.
Но еще больше удивились они, когда Рэлей заявил, что берется доказать существование аргона при помощи… трубок для курения табака! Рэлей тут же взял восемь таких трубок – восемь прямых коротких трубок из обожженной глины, какие курят англичане, – и соединил их гуттаперчевыми креплениями. Получилась одна прямая и длинная труба. Он вставил ее в стеклянный сосуд, соединенный с воздушным насосом: труба входила в сосуд через отверстие в крышке, а выходила через отверстие в дне.
Все щели прибора Рэлей тщательно залил сургучом.
Потом он принялся гнать по трубе добытый из воздуха азот.
Азот втекал в один конец трубы, а из другого вытекал в газометр. Но вытекал не весь, – большая часть его терялась по дороге. Ведь обожженная глина – это пористый материал со множеством микроскопических трещинок и лазеек. Через эти-то лазейки азот и просачивался наружу – в сосуд. А для того, чтобы он просачивался еще быстрее, из сосуда все время выкачивали воздух. Лишь ничтожным остаткам азота удавалось пройти через трубу от одного конца до другого и попасть в газометр.
Рэлей взял из газометра кубический сантиметр газа и на глазах у химиков взвесил его. Оказалось, что он был на целых двенадцать-пятнадцать процентов тяжелее, чем кубический сантиметр обыкновенного азота.