Выше было показано, что именно ядро, — атомный остов, своей бипирамидальной формой задаёт все свойства атомов и отвечает за периодичность свойств элементов, проявляющуюся в форме периодического закона Д.И. Менделеева (§ 3.3). Тем самым, впервые проложен мост между химическими и ядерными свойствами элементов, о чём давно мечтали физики [139, 145]. Но, оказывается, связь химических и ядерных свойств проявляется и в другом. Так, ядерные свойства элементов тоже имеют некую периодичность, во многом повторяющую периодичность химических свойств. Это видно из распространённости элементов, числа их изотопов, значений атомных масс. Скачки этих характеристик обычны на границах периодов. Поэтому, заметно выбиваются из общей последовательности элементы VIIIA группы, — инертные газы: He, Ne, Ar, Kr, Xe, Rn (Рис. 106), — хотя бы по резким скачкам их атомных масс. Если проследить зависимость атомного веса от номера элемента, нанеся её на график, то получится монотонная кривая: атомный вес, с увеличением номера на единицу, возрастает в среднем на две единицы. Но есть на этой кривой выбросы, скачки, — особенно заметные вблизи инертных газов. Рекорд принадлежит радону, со скачком аж на 12 атомных единиц массы.
Периодичность свойств атомов — это, как нашли выше, следствие послойного заполнения бипирамидального остова (ядра) атома электронами (§ 3.3). Когда заполнится один слой, прочно связанные в нём электроны уже не отрываются и не участвуют в образовании химической связи, и, при заполнении следующего слоя, всё повторяется с нуля. Оттого, и свойства элементов периодически повторяются с заполнением каждого последующего уровня. Тем же, видимо, обусловлена и некая периодичность свойств ядер, проявляющаяся в существовании магических ядер (особо устойчивых сочетаний нуклонов, аналогичных химически устойчивым атомам инертных газов), а, также, — связь между свойствами ядер и расположением элементов в таблице Менделеева.
Так, к примеру, по неясной причине, повышена стабильность ядер у элементов IA группы. В ней больше всего стабильных нечётно-нечётных ядер. Подобные ядра, содержащие нечётное число протонов и нейтронов, обычно, — крайне нестабильны и потому не встречаются в природе. Известно лишь 4 стабильных нечётно-нечётных ядра, но, из этих четырёх, два расположены в первой группе: 2H, 6Li, так же, как нечётно-нечётное ядро 40K, имеющее столь большой период полураспада, что прежде оно считалось стабильным и до сих пор может условно считаться таковым. На деле, калий-40 относят к естественно-радиоактивным изотопам, имеющим огромный период полураспада, а, потому, всё же сохранившимся в природе. Число естественно-радиоактивных ядер невелико, и, опять же, их больше всего в IA группе: кроме 40K, это 87Rb, 135Cs и 223Fr. Химический антипод элементов первой группы — элементы седьмой группы. Но и по ядерным свойствам это — антипод. Так, видимо, от низкой стабильности ядер в природе редко встречаются или напрочь отсутствуют элементы VIIB группы. Этот закон, открытый ещё в 1924 г. В. Прандтлем и А. Гриммом, был забыт, как и всё противоречащее квантовой теории [145]. В самом деле, из пяти элементов группы VIIБ (по исконному варианту таблицы Менделеева и Браунера, Рис. 109): Mn, Tc, Re, Pm и Np, — распространён только марганец, рений же крайне редок (это самый дорогой металл), а все прочие элементы, будучи нестабильны, в природе практически не встречаются и их получают искусственным путём.
Другой пример дают нестабильные нечётно-нечётные ядра с очень большим периодом полураспада. В природе можно встретить лишь 4 таких ядра: 40K, 50V, 138La, 176Lu. Но, ведь, La и Lu — это крайние элементы ряда лантаноидов, а K и V — крайние элементы полупериметра 4-го слоя (Рис. 109). Исключительность элементов из семейства лантана (лантаноидов), не только в плане химических, но и в плане ядерных свойств, отмечалась уже давно [145]. Но никто не мог объяснить, почему эти свойства взаимосвязаны. А причина, как увидим, — в их едином механизме, в атомном остове. Кристаллический ядерный остов атома и осуществляет связь химических свойств элементов, их положений в таблице Менделеева — с их ядерными свойствами. О такой связи говорили ещё И. Ридберг, А. Ван-ден-Брук, Ф. Содди [139], которые закладывали основы представлений о строении атома, ядра и защищали исконную форму таблицы Менделеева, где лантаноиды и актиноиды распределены по группам ( Лисневский Ю. Антониус Ван-ден-Брук. М.: Наука, 1981).
Всё перечисленное подтверждает тесную связь строения ядра и электронных слоёв в атоме. Выходит, таблица Менделеева отражает закономерности, чередование и взаимосвязь не только физико-химических, но и ядерных свойств элементов. Значит, бипирамидальный остов атома отвечает как-то и за ядерные свойства элементов. Таким образом, именно эта геометрическая структура бипирамиды должна дать ключ к пониманию структуры ядра. Геометрия, наглядный, образный подход, как знает любой инженер, позволяют легко решать даже задачи, непокорные аналитическим методам. Именно так Луи Пуансо — инженер, известный открытием нового типа правильных многогранников, — решил важную проблему механики. Без геометрии невозможны адекватные представления о строении мира. Так, пространственное размещение атомов в молекулах и кристаллах определяет их физико-химические свойства, а размещение элементов в таблице Менделеева — даёт информацию о свойствах атомов и их соединений. Но, по иронии судьбы, именно в микромире, — фундаменте мироздания, — геометрию и наглядные модели игнорируют, считают ненужными, сводя всё к формулам и прикрываясь туманом неопределённости, абсурдной размытости частиц, лишающей мир чёткой структуры.
Наглядный, а, точней, "ненаглядный" пример этого дают нынешние представления об атомном ядре. Его изображают то заряженной каплей, то чередой оболочек, то ещё чем-нибудь, а то и, вовсе, — сгустком формул [11]. В итоге, физики так запутались, что сами признают своё непонимание структуры ядра и бессилие квантовой теории [135]. И лишь классическая модель атома даёт кристально ясную структуру ядра, объясняющую все его свойства. В этой модели ядро атома имеет вид бипирамиды: двух пирамид, соединённых усечёнными вершинами. Сия структура и задаёт конфигурацию электронных слоёв (оболочек), связь химических и ядерных свойств. Так, подобно атомам инертных газов, с особо устойчивыми конфигурациями электронов и высокой химической стойкостью, в некоторых ядрах нуклоны (протоны и нейтроны) образуют особо устойчивые сочетания, проявляющие инертность в ядерных реакциях. Такие ядра, названные "магическими", имеют повышенную прочность и слабо реагируют с другими ядрами и нейтронами.
Вот числа протонов или нейтронов, образующих особо прочные сочетания (магические числа): 2, 8, 14, 20, 28, 50, 82, 126 [169]. Физики поняли, что магические числа, подобно периодам таблицы Менделеева, вызваны присутствием в ядре неких слоёв, оболочек, постепенно заполняемых нуклонами (протонами и нейтронами). Магичны и особо стабильны ядра с целиком укомплектованными оболочками. Но физики не сделали последнего шага: не догадались, что строение ядерных и электронных слоёв задано одной и той же структурой, — атомным ядром, которое и ответственно за глубокую аналогию химических и ядерных свойств, их периодичность.
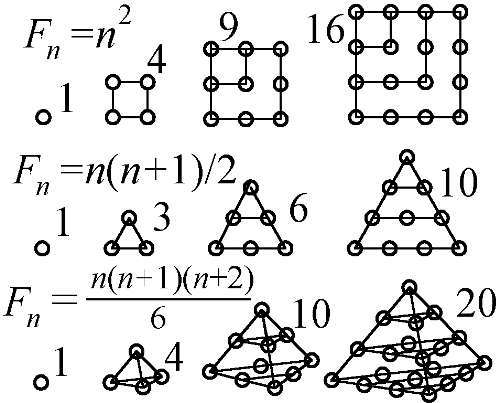
Рис. 110. Фигурные числа (квадратные, треугольные) и пирамидальные числа.
Эта аналогия объясняет строение слоёв ядра. Числа электронов в электронных оболочках (2, 8, 18, 32) — это удвоенные квадраты целых чисел: 1 2, 2 2, 3 2, 4 2(§ 3.3). В геометрии такие числа n 2называют "квадратными", относя к группе фигурных чисел, — количеств одинаковых камешков, частиц, послойно заполняющих фигуры в виде треугольников, квадратов и т. д. (Рис. 110). Так, треугольные числа образуют ряд: 1, 3, 6, 10…, где n-ое число F n= n( n+1)/2. И, если числа электронов в слоях — это удвоенные квадратные числа, то числа протонов или нейтронов в ядерных оболочках оказались удвоенными треугольными числами вида n( n+1), то есть 2, 6, 12, 20, 30, 42, 56 [135]. Отсюда следуют все магические числа. Первое число 2 соответствует первому целиком заполненному нуклонами слою с числом мест 2. Второе магическое число 8 означает, что кроме первого заполнен ещё и второй слой из 6-ти мест: 2+6=8. Магическое число 20 возникает, если заполнен ещё и третий уровень: 2+6+12=20. Как для случая электронных слоёв, ядерные укладываются один над другим — в виде пирамиды, а, потому, эти три числа — это удвоенные пирамидальные числа вида n( n+1)( n+2)/3, образующие ряд: 2, 8, 20, 40, 70. Прочие магические числа находятся как удвоенная сумма n-го треугольного числа и ( n–2) — го пирамидального: n( n+1)+ n( n—1)( n—2)/3=( n 3 +5 n)/3 (Рис. 111) [169].