Дискретный набор энергетических уровней
Существует дискретный набор энергетических уровней для данных значений массы m и размера ящика L. Поскольку квантовое число n принимает значения 1, 2, 3 и т. д., соответствующие значения энергии будут равны
h2/8∙m∙L2, 4∙h2/8∙m∙L2, 9∙h2/8∙m∙L2, и т. д.
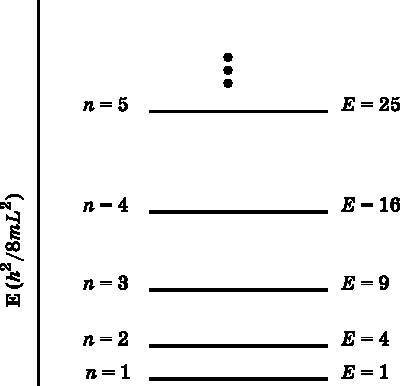
Рис. 8.6. Энергетические уровни частицы в ящике. Здесь n — квантовое число, а E — энергия, которая увеличивается как квадрат квантового числа. Энергия выражена в единицах h2/8∙m∙L2, так что хорошо видно, как она возрастает. Штриховой линией обозначена нулевая энергия. Самый низкий энергетический уровень не совпадает с линией E=0 в отличие от случая классической частицы в ящике
На рис. 8.6 представлена диаграмма энергетических уровней для первых нескольких значений энергии частицы в ящике. Энергия выражена в единицах h2/8∙m∙L2. Чтобы получить фактическое значение энергии, нужно просто подставить конкретные значения m и L в формулу для энергетических уровней. На диаграмме видно, что энергия увеличивается как квадрат квантового числа n. Штриховой линией обозначено, где энергия равна нулю. Квантовая частица в ящике на наинизшем энергетическом уровне имеет ненулевую энергию, чем резко отличается от классической частицы в ящике. На классической ракетбольной площадке энергия, которой может обладать мяч, непрерывна. Ударяя по мячу чуть сильнее или чуть слабее, его энергию можно увеличить или уменьшить на любую величину. Однако в квантовом ракетболе возможны лишь отдельные значения энергии, показанные на рис. 8.6. Как отмечалось в начале нашего разговора о квантовой частице в ящике, наименьшая энергия не равна нулю. Если бы квантовая частица в ящике могла иметь нулевую энергию, это нарушало бы принцип неопределённости.
Связь результатов для частицы в ящике с реальными системами
Частица в ящике — это очень простая иллюстрация общего свойства абсолютно малых систем. Энергия таких систем не обязательно непрерывна. Частица в ящике не является физически реализуемой системой, поскольку она одномерна и окружена «идеальными» стенками. Однако атомы и молекулы — реальные системы. Энергетические уровни атомов и молекул исследовались очень подробно, а их квантованные энергетические уровни измерялись экспериментально и рассчитывались теоретически. Подобно тому как энергетические уровни частицы в ящике зависят от свойств системы (массы частицы и длины ящика), энергетические уровни в атомах и молекулах зависят от свойств этих атомов и молекул.
Молекулы поглощают свет определённых цветов
Хотя частица в ящике не является физически реализуемой системой, свойства, обнаруженные в этой задаче, также присущи атомам и молекулам. При фотоэлектрическом эффекте энергия падающих фотонов столь велика, что из куска металла выбиваются электроны (см. главу 4). При достаточно большой энергии фотона его удар по молекуле также может привести к выбросу электрона. Однако в случае более низкой энергии фотонов при падении света на атом или молекулу он может поглощаться без испускания электронов. Внутренняя энергия атома или молекулы при этом возрастает, поскольку к ней добавляется энергия фотона.
Молекулы (и атомы) состоят из заряженных частиц: электронов, заряженных отрицательно, и атомных ядер, несущих положительный заряд. В видимом и ультрафиолетовом диапазонах, то есть при длине волны менее 700 нм, частота света очень велика. Колеблющееся электрическое поле света взаимодействует с заряженными частицами молекул. Электроны очень лёгкие, и поэтому им проще откликнуться на быстрые колебания электрического поля света видимого или ультрафиолетового диапазона. Поглощение видимого излучения и ультрафиолета вызвано увеличением энергии электронов в молекуле.
Вопрос состоит в том, какова длина световых волн, которые будут поглощаться молекулой? Это очень сложный вопрос для любой конкретной молекулы. Чтобы теоретически определить спектр поглощения молекулы, приходится выполнять огромное количество квантовомеханических расчётов. Тем не менее важные аспекты молекулярного поглощения света можно разобрать на основе задачи о частице в ящике. В качестве чрезвычайно упрощённой модели молекулы мы будем рассматривать одиночный электрон в ящике молекулярного размера. В конце мы подставим в формулы числа. Когда на электрон, находящийся в ящике (молекуле), никакой свет не падает, он пребывает в состоянии с наименьшей энергией, так называемом основном состоянии. Для частицы в ящике наименьшей энергии соответствует квантовое число n=1. При n=1
E=h2/8∙m∙L2.
Когда на молекулу попадает свет, фотон может быть поглощён. В этом случае общая энергия света убывает на величину энергии поглощённого фотона. Энергия должна сохраняться, что обеспечивается переходом электрона в более высокое энергетическое состояние, то есть он покидает основное состояние с наименьшим уровнем энергии и переходит на более высокий энергетический уровень. Однако этот более высокий энергетический уровень не может иметь произвольное значение энергии, поскольку энергетические уровни частицы в ящике (и в молекулах) квантуются. Самое низкое энергетическое состояние над основным уровнем соответствует квантовому числу n=2. Это состояние называется первым возбуждённым. Электрон возбуждается при поглощении фотона и переходит из основного состояния в первое возбуждённое. Энергия первого возбуждённого состояния (n=2) равна
E=4∙h2/8∙m∙L2.
Энергия должна сохраняться. Это верно для классической механики и остаётся верным в квантовой механике. Вначале электрон находился в основном состоянии. Затем, после поглощения фотона, перешёл в возбуждённое состояние. Следовательно, для того чтобы соблюдался закон сохранения, энергия фотона должна быть равна разности между энергией возбуждённого состояния электрона и энергией его основного состояния. Только фотон с такой энергией может быть поглощён данной системой. Энергия фотона определяется длиной волны света. Следовательно, поглощаться может свет только некоторых определённых цветов.
Рисунок 8.7 иллюстрирует поглощение фотона. Стрелки показывают два разрешённых пути, по которым может поглотиться фотон. Их называют переходами. На рисунке отражены переходы из n=1 в n=2 и из n=1 в n=3. Чтобы фотон был поглощён, его энергия должна быть равна разности энергий двух квантовых уровней. Если энергия фотона не совпадает с разностью энергий двух квантовых уровней, он не может поглотиться.
Разность энергий ∆E между энергетическим уровням перового возбуждённого состояния (n=2) и энергетическим уровнем основного состояния (n=1) равна
∆E=(4∙h2/8∙m∙L2)−(h2/8∙m∙L2),
∆E=3∙h2/8∙m∙L2.
Это энергия, которую должен иметь фотон, чтобы заставить электрон совершить переход из основного состояния в первое возбуждённое. Можно воспользоваться соотношением Планка E=h∙ν для энергии фотона, чтобы убедиться в том, что энергии ∆E соответствует определённая частота света. Кроме того, поскольку произведение длины волны и частоты равно скорости света λ∙ν=c, можно найти длину волны (цвет) того света, который будет испытывать поглощение.