Таблица (продолжение)
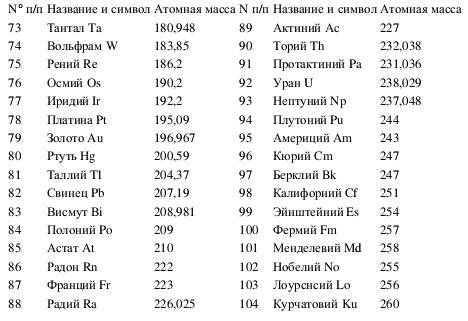
| N° п/п | Название и символ | Атомная масса | N п/п | Название и символ | Атомная масса |
| 73 | Тантал Та | 180,948 | 89 | Актиний Ас | 227 |
| 74 | Вольфрам W | 183,85 | 90 | Торий Th | 232,038 |
| 75 | Рений Re | 186,2 | 91 | Протактиний Pa | 231,036 |
| 76 | Осмий Os | 190,2 | 92 | Уран U | 238,029 |
| 77 | Иридий Ir | 192,2 | 93 | Нептуний Np | 237,048 |
| 78 | Платина Pt | 195,09 | 94 | Плутоний Pu | 244 |
| 79 | Золото Au | 196,967 | 95 | Америций Am | 243 |
| 80 | Ртуть Hg | 200,59 | 96 | Кюрий Cm | 247 |
| 81 | Таллий Tl | 204,37 | 97 | Берклий Bk | 247 |
| 82 | Свинец Pb | 207,19 | 98 | Калифорний Cf | 251 |
| 83 | Висмут Bi | 208,981 | 99 | Эйнштейний Es | 254 |
| 84 | Полоний Ро | 209 | 100 | Фермий Fm | 257 |
| 85 | Астат At | 210 | 101 | Менделевий Md | 258 |
| 86 | Радон Rn | 222 | 102 | Нобелий No | 255 |
| 87 | Франций Fr | 223 | 103 | Лоуреснсий Lo | 256 |
| 88 | Радий Ra | 226,025 | 104 | Курчатовий Ku | 260 |
Примером может служить хлор, атомная масса которого равна 35,453 (в таблице Берцелиуса, составленной в 1826 году, атомная масса хлора 35,4). Поэтому гипотеза Праута в том виде, в каком он её сформулировал, безусловно должна быть отброшена.
Заметим всё же, просматривая нашу таблицу, что очень многие атомные массы, особенно в начале таблицы, весьма близки к целым числам, иногда в точности им равны, например, у фтора и углерода, а иногда отличаются от них меньше чем на 0,01, например, у водорода, гелия, азота, натрия и т. д. Это странное обстоятельство заставляет как будто отнестись с некоторым вниманием к гипотезе Праута[7], так как трудно себе представить, чтобы это могло быть результатом чистого случая, но тем не менее такие атомные массы, как у магния или хлора, не говоря уже о многочисленных элементах с большими атомными массами, всё-таки принуждают отбросить предположение о том, что все атомы состоят из атомов водорода.
Поэтому в XIX столетии совершенно укрепилось и распространилось представление о том, что все тела в мире состоят из этих нескольких десятков сортов атомов, которые являются совершенно независимыми друг от друга основными элементами мироздания. Атомы вечны и неразрушимы и не могут превращаться друг в друга.
«Даже когда Солнечная система распадётся и на её развалинах возникнут другие миры, атомы, из которых она состоит, останутся целыми и неизношенными»,
— так сказал в 1873 году в одной речи знаменитый английский физик Джемс Клерк Максвелл, основатель современной теории электрического и магнитного полей. Из этой цитаты видно, как нераздельно властвовали в физике идеи Дальтона даже через несколько десятилетий после появления его «Химической философии».
И всё же, несмотря на всё это, среди физиков и химиков продолжало жить смутное убеждение в том, что между атомами различных химических элементов имеются какие-то связи, что эти атомы образуют какую-то естественную систему. Удивительно, что эта мысль была отчётливо сформулирована ещё задолго до того, как стало известно, какие именно химические элементы существуют в природе. В 1786 году немец Н.Г.Марне напечатал книгу, озаглавленную «О числе элементов». В этой книге, мистической и странной, он выражает своё глубокое убеждение в том, что «от мельчайшей пылинки солнечного пуча до святейшего серафима можно воздвигнуть целую лестницу творений» и что атомы химических элементов тоже являются ступенями этой лестницы. Марне продолжает:
«Подобно тому, как каждый отдельный тон созвучен тому же тону октавой выше или ниже вследствие связи между числом колебаний струн, так же и определённые химические элементы („основные вещества“, как называет их Марне) могут по тем же причинам стоять в самом близком родстве друг с другом, несмотря на то, что в их естественной последовательности между ними находятся многие вещества: с этими веществами они так же не могут соединиться, как два тона не могут приятно звучать вместе, несмотря на свою близость, если они находятся в отношении секунды».
Эта идея Марне не могла привести ни к каким последствиям, пока химические элементы не были в достаточной мере выделены и изучены. Но после того, как Канниццаро опубликовал (в 1858 году) свою таблицу атомных масс, стремление к естественной классификации химических элементов должно было принести свои плоды.
7
Отступления от целочисленности связаны с существованием изотопов одного и того же химического элемента таблицы Менделеева, различающихся атомными массами. Открытие изотопов подтвердило правильность гипотезы Праута, (Прим. ред.)