Следующая весьма грубая картина позволит нам хотя бы в общих чертах понять, как ведут себя волны электронов в представлении Шрёдингера. На рис. 38 показана часть волны протяженностью 2λ.Если такую волну создать, проведя смычком по скрипичной струне, то она будет колебаться вверх-вниз, занимая положения, показанные сплошной и штриховой кривыми. Можно возбудить и некую последовательность волн, длины которых составляют лишь дробные части основной длины волны (например, половину и треть ее). В представлении Шрёдингера полная волна, соответствующая любому электрону, окружая ядро, может простираться на две, три и даже пять основных длин волн. В каждом случае в полной волне электрона укладывается целое число основных волн и конец последней волны совпадает с началом первой (на рис. 38 точка Bдолжна совпадать с точкой A)
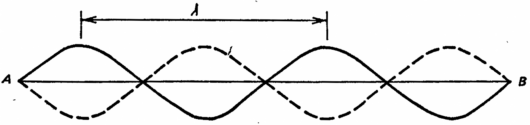
Рис. 38.
Введенная Шрёдингером ψ-функция задает амплитуду волн материи, изменяющихся от точки к точке и от одного момента времени к другому. Это стоячие волны, сосредоточенные преимущественно в небольшой области пространства вблизи ядра. По мере увеличения расстояния от ядра волны постепенно затухают, но амплитуда их остается отличной от нуля в области, размеры которой совпадают с экспериментально установленными размерами соответствующего атома. Например, для атома водорода, находящегося в основном (самом нижнем) энергетическом состоянии, амплитуда волн заметно отлична от нуля только в пределах сферы диаметром около 10 −8см. Для любого атома решение волнового уравнения Шрёдингера позволяет получить дискретный набор волн атомных электронов, и с каждым состоянием атома оно связывает определенное значение энергии.
Подчеркнем еще раз, что волна Шрёдингера, описывающая электрон в атоме, представляет не простую волну с одной-единственной частотой, а состоит из целого набора волн с различными частотами. В этом отношении волна Шрёдингера аналогична сложным звуковым волнам, создаваемым музыкальными инструментами.
В связи с волнами де Бройля — Шрёдингера естественно напрашивается вопрос: из чего они «сделаны», или, иначе говоря, из чего они состоят? Подобный вопрос вставал перед физиками и в XIX в., когда было открыто световое и другие виды электромагнитного излучения. Сначала физики полагали, что электромагнитные волны представляют собой колебания таинственной субстанции, называемой эфиром, и придумывали различные механические модели, объясняющие действие эфира. Но со временем физики поняли несостоятельность такого рода идей и стали считать электромагнитные волны самостоятельными сущностями. Нечто похожее произошло и с волнами электронов. Первоначально Шрёдингер предположил, что эти волны действительно описывают распределение заряда электрона, т.е. что в атоме заряд и плотность электрона физически распределены в той области пространства, где амплитуда волны отлична от нуля. Но ничего подобного не наблюдалось. Наоборот, после открытия электрона выяснилось, что весь его заряд сосредоточен в небольшой области пространства и что электрон имеет корпускулярную природу.
Строго говоря, когда мы рассуждаем о возможных видах волн, соответствующих различным энергетическим состояниям электрона, то имеем в виду один электрон, не испытывающий воздействия других частиц. Если же в атоме много электронов, то они утрачивают свою «индивидуальность» и соответствующие им волны сливаются в общую волну, «одну на все электроны».
В представлении Шрёдингера электроны подобны облакам с переменной плотностью. Они трехмерны. Электронные облака образуют несколько «ярусов» вокруг ядра. Плотность каждого облака возрастает от нуля до максимума и снова убывает до нуля. Электронные облака простираются и за пределы атома, но для каждого электрона их плотность максимальна на таком расстоянии от ядра, которое предсказывается теорией Бора. Электронное облако как интерпретация абстрактного математического понятия с неизбежностью неточно. Представить себе наглядно без ущерба для точности ψ-функцию Шрёдингера невозможно. Нахождение аналитических решений уравнения Шрёдингера — задача настолько трудная, что решить ее удается лишь в отдельных исключительных случаях. Тем не менее полученные решения превосходно согласуются с экспериментальными данными, а другие решения, хотя и приближенные, также достаточно хорошо соответствуют результатам экспериментов. В частности, удалось полностью решить уравнение Шрёдингера для случая атома водорода. Полученное решение позволяет ответить на любой вопрос, допускающий экспериментальную проверку.
То, что электроны при определенных условиях ведут себя как волны, было продемонстрировано в 1927 г. знаменитым экспериментом Клинтона Дж. Дэвиссона (1881-1958) и Лестера Джермера (1896-1971) и независимо Джорджем П. Томсоном (1892-1975). Все эти исследователи обнаружили дифракцию электронов (в качестве дифракционной решетки использовался кристалл) Дифракция как явление, состоит в том, что волны огибают встречающееся на пути препятствие и заходят за него в область «тени». Нечто подобное мы наблюдаем, когда волны на воде огибают корпус судна. Опыты Дэвиссона и Джермера, а также Томсона показали, что в некоторых случаях частицы ведут себя как волны. Физики окончательно убедились в том, что всем субатомным частицам соответствуют свои волны, длины которых определяются формулой де Бройля. Так, работы де Бройля и Шрёдингера выдвинули на передний план понятие корпускулярно-волнового дуализма (волна — частица), доставившее немало хлопот и физикам, и философам.
Несмотря на экспериментальное подтверждение того, что электроны при определенных условиях ведут себя как волны, далеко не все физики смирились с представлением об электронах, «размазанных» вокруг атомного ядра. Некоторые усматривали, в частности, противоречие в следующем: с одной стороны, в любой физически бесконечно малой области плотность заряда электрода должна быть бесконечно мала, а с другой — электрический заряд электрона является величиной вполне определенной. Все электрические заряды кратны заряду электрона. Руководствуясь этими соображениями и пытаясь избежать корпускулярно-волнового дуализма, Макс Борн (1882-1970) в 1926 г. предложил совершенно иную интерпретацию теории Шрёдингера: ввел ее вероятностную интерпретацию.
Теория вероятностей вошла в математику благодаря случаю, а именно в связи с задачами об азартных играх. Но в конце XIX в. Максвелл и Людвиг Больцман (1844-1906), воспользовавшись в своих исследованиях вероятностными соображениями, пришли к законам, описывающим движение газов, — к кинетической теории газов. Одна из знаменитых работ, опубликованных Эйнштейном в 1905 г., также была посвящена вероятностной задаче о так называемом броуновском движении. Вместо того чтобы рассматривать электрон как распределенный в некоем пространственном облаке, плотность которого меняется от точки к точке, Борн интерпретировал плотность как вероятность обнаружить электрон как частицу в той или иной точке пространства.
Обращаясь к ψ-функции, входящей в дифференциальное уравнение Шрёдингера, Борн предложил трактовать величину ψкак вероятность того, что частица находится в данном элементе пространства в данный момент времени. Следовательно, местонахождение электронов как частиц может быть указано лишь с большей или меньшей вероятностью. Например, если в некоторой области пространства |ψ| 2= 0,8, то вероятность обнаружить частицу (электрон) в ней составляет 80 шансов из 100. Вероятностная интерпретация Борна общепринята и поныне.
Такой подход позволяет точно оценивать, с какой вероятностью электрон может находиться в любом данном объеме. При подобной интерпретации электрон локализован, а не «размазан», как в волновой механике Шрёдингера. Тем не менее остается вопрос, является ли вероятностная интерпретация наилучшей из возможных или же она просто порождена неполнотой наших представлений об электроне.