Цинк, как известно, образует только одно соединение с хлором — хлористый цинк ZnCl2, медь же — два: хлорную медь CuCl2 и хлористую медь Cu2Cl2. Явление происходит, следовательно, таким образом, что слабый ток отрывает от электрода на каждые два атома хлора два атома меди, которые остаются связанными между собой при помощи одной из двух своих единиц сродства, между тем как две их свободные единицы сродства соединяются с двумя атомами хлора:
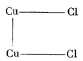
Если же ток становится сильнее, то он совершенно отрывает атомы меди друг от друга, и каждый из них в отдельности соединяется с двумя атомами хлора:
При токах средней силы оба эти вида соединений образуются рядом друг с другом. Таким образом, образование того или другого из этих соединений зависит исключительно лишь от силы тока, и поэтому весь процесс носит по существу электро-химический характер, если это слово имеет вообще какой-нибудь смысл. Несмотря на это, Видеман категорически объявляет его вторичным, т. е. не электро-химическим, а чисто химическим процессом.
Вышеприведенный опыт принадлежит Рено (1867 г.) и относится к целому ряду аналогичных опытов, в которых один и тот же ток проводился в U-образной трубке через раствор поваренной соли (положительный электрод — цинк), а в другой ванне через различные электролиты с различными металлами в качестве положительных электродов. При этом растворенные на один эквивалент цинка количества других металлов показали большие отклонения, и Видеман приводит результаты всего ряда опытов, которые, однако, в большинстве случаев химически вполне понятны и никак не могут быть иными. Так, например, на 1 эквивалент цинка в соляной кислоте растворялось только 2/3 эквивалента золота. Это может казаться странным лишь в том случае, если, подобно Видеману, придерживаться старых эквивалентных весов и изображать хлористый цинк через ZnCl, где как хлор, так и цинк фигурируют в хлористом соединении каждый только с одной единицей сродства. В действительности же здесь на один атом цинка приходится два атома хлора (ZnCl2), и, зная эту формулу, мы сразу же видим, что в вышеприведенном определении эквивалентов за единицу надо принимать атом хлора, а не атом цинка. Формулу же для хлорного золота надо писать AuCl3; в этом случае ясно, что 3ZnCl2 содержат ровно столько же хлора, сколько 2AuCl3, и что поэтому все процессы в цепи или электролитической ванне (первичные, вторичные и третичные) вынуждены будут на одну превращенную в хлористый цинк весовую часть[349] цинка превращать в хлорное золото не больше и не меньше чем 2/3 весовой части золота. Это имеет абсолютное значение, если только не предположить, что гальваническим путем можно получить также и соединение AuCl: в этом последнем случае на 1 эквивалент цинка должны были бы быть растворены даже 2 эквивалента золота, и, следовательно, могли бы иметь место, в зависимости от силы тока, такие же вариации, какие были указаны выше на примере меди и хлора. Значение опытов Рено заключается в том, что они показывают, как закон Фарадея подтверждается фактами, как будто бы противоречащими ему. Но совершенно непонятно, какое значение они должны иметь для объяснения вторичных процессов при электролизе.
Третий пример Видемана привел нас уже опять от электролитической ванны к цепи. И действительно, наибольший интерес представляет цепь, если исследовать электролитические процессы с точки зрения происходящих при этом превращений энергии. Так, мы нередко наталкиваемся на такие цепи, в которых химико-электрические процессы как будто находятся в прямом противоречии с законом сохранения энергии и совершаются как будто вопреки законам химического сродства.
Согласно измерениям Поггендорфа[350], цепь: цинк, концентрированный раствор поваренной соли, платина — дает ток силой в 134,6 [Пометка на полях: «Если принять, что сила тока 1 элемента Даниеля = 100». Ред.]. Таким образом, мы имеем здесь довольно солидное количество электричества, на 1/3 больше, чем в элементе Даниеля. Где же источник появляющейся здесь в форме электричества энергии? «Первичным» процессом является здесь вытеснение цинком натрия из его соединения с хлором. Но в обычной химии не цинк вытесняет натрий из хлористых и других соединений, а, наоборот, натрий вытесняет цинк. «Первичный» процесс не только не в состоянии дать току вышеуказанного количества энергии, но, наоборот, сам нуждается для своего осуществления в притоке энергии извне. Таким образом, с одним лишь «первичным» процессом мы опять-таки не двигаемся с места. Поэтому рассмотрим, как процесс происходит в действительности. Мы находим, что происходящее здесь превращение выражается не через
Zn + 2NaCl = ZnCb + 2Na,
а через
Zn + 2NaCl + 2H2O = ZnCl2 + 2NaOH + H2. Иными словами: натрий не выделяется в свободном виде на отрицательном электроде, а превращается в гидрат окиси, как выше в примере I (стр. [459—460]).
Для вычисления происходящих при этом превращений энергии мы имеем по меньшей мере опорные пункты в определениях Юлиуса Томсена. Согласно им, мы имеем следующее количество освободившейся энергии при соединениях:
(Zn, Cl2) = 97 210 (ZnCl2, aqua) = 15 630 итого для растворенного ZnCl2 : 112840 единиц теплоты
2 (N, O, H, aqua) = 223 620 » »
336 460 » »
Отсюда надо вычесть количество энергии, потраченное при разделениях:
329 740 » »
Избыток освободившейся энергии = 6720 единицам теплоты.
Этого количества, конечно, мало для полученной Поггендорфом силы тока, но его достаточно, чтобы объяснить, с одной стороны, отделение натрия от хлора, а с другой — образование тока вообще.
Здесь перед нами поразительный пример того, что различие между первичными и вторичными процессами вполне относительно и что оно приводит нас к абсурду, если мы станем его рассматривать как нечто абсолютное. Если брать первичный электролитический процесс сам по себе, изолированно, то он не только не может породить тока, но он и сам не может совершаться. Только вторичный, якобы чисто химический процесс впервые делает возможным первичный процесс, доставляя сверх того весь избыток энергии, необходимый для образования тока. Таким образом, он оказывается в действительности первичным процессом, а «первичный» оказывается вторичным. Когда Гегель, выступая против метафизиков и против метафизически мыслящих естествоиспытателей, диалектически превращал выдуманные ими неподвижные различия и противоположности в нечто обратное тому, что они утверждали, то его обвиняли в том, что он извращает их слова. Но когда природа поступает с этими различиями и противоположностями так же, как старик Гегель, то не пора ли несколько ближе исследовать это дело?
С большим правом можно считать вторичными те процессы, которые, хотя и происходят вследствие химико-электрического процесса в цепи или электро-химического процесса в электролитической ванне, но совершаются независимо и отдельно от него, т. е. те процессы, которые имеют место на некотором расстоянии от электродов. Поэтому совершающиеся при подобных вторичных процессах превращения энергии и не вступают в электрический процесс; они ни отнимают у последнего, ни доставляют ему прямым образом энергию. Подобные процессы встречаются в электролитической ванне очень часто; выше под № I мы имели пример этого в образовании серной кислоты при электролизе сернокислого натрия. Но в электролитической ванне они представляют меньше интереса. Зато гораздо более важно с практической стороны появление их в цепи, ибо хотя прямым образом они и не доставляют энергию химико-электрическому процессу и не отнимают ее у него, но всё же они изменяют общую сумму имеющейся в цепи энергии, воздействуя благодаря этому на химико-электрический процесс косвенным образом.